在前几篇文章里,我们讨论了一个核心问题:
究竟是谁在决定一个基因“怎么剪”?
研究者通常会先通过转录组数据发现某个基因存在可变剪接,然后进一步寻找可能参与调控的 RNA结合蛋白(RNA-binding proteins,RBP)。通过 motif 分析、CLIP-seq 或表达数据,往往可以锁定一批候选调控因子。
但当研究推进到这里时,一个关键问题仍然没有解决:
这些RBP,真的在直接调控这个剪接事件吗?
换句话说,我们需要进一步回答:
-
哪一段 RNA 序列在发挥作用?
-
某个 RBP 是否通过这段序列影响剪接?
-
某个突变是否会改变剪接模式?
在绝大多数剪接机制研究中,用来回答这些问题的经典实验工具就是:
minigene。
从概念上看,minigene其实是一个 人工构建的剪接报告系统。 研究者会从目标基因中截取一段关键区域,通常包括: 一个目标外显子 上下游部分内含子 邻近外显子 然后将这段 DNA 片段克隆到表达载体中,在细胞中表达。 当该载体在细胞中转录后,会像天然基因一样经历: 转录 → pre-mRNA → RNA剪接 研究者随后通过 RT-PCR 或测序,就可以观察这段 RNA 在细胞中的剪接结果。 因此,minigene的核心价值在于: 在可控条件下“重建一个剪接事件”。 在真实基因组中,剪接调控往往受到很多因素影响,例如: 染色质状态 转录速率 RNA结构 多个RBP的协同作用 这些因素叠加在一起,很难直接判断 到底是哪一段序列在决定剪接选择。 而 minigene 可以将复杂系统简化,让研究者能够单独测试: 某段序列是否是剪接调控元件 某个突变是否改变剪接 某个RBP是否参与调控 这也是为什么在很多剪接机制研究论文中,minigene几乎是必做实验。
minigene:在细胞中“重建一个剪接事件”
一个案例:minigene如何帮助解析剪接机制?
在一项关于口腔鳞状细胞癌(OSCC)的研究中,研究者发现 SLC37A4 基因存在异常的可变剪接事件,并进一步证明剪接因子 SRSF9 通过调控这一剪接过程促进肿瘤进展。 研究最初来自 转录组数据分析。研究者对口腔癌组织和正常组织进行了 RNA-seq 数据比较,在分析剪接事件时发现,SLC37A4 的 exon7 在肿瘤样本中频繁发生跳跃(exon skipping)。这一剪接改变会产生一个新的转录本亚型 SLC37A4-S。随后通过 RT-PCR 和 Sanger 测序,研究者在细胞系中验证了这一剪接形式的存在,并发现该剪接亚型在肿瘤组织中显著升高。 接下来,研究者进一步探究这一剪接事件的功能。通过 构建不同剪接亚型的表达载体并进行过表达实验,他们发现 SLC37A4-S 可以明显促进肿瘤细胞的增殖、迁移和侵袭能力,提示这一剪接事件可能具有促癌作用。 既然这一剪接变化具有功能意义,下一个关键问题就是:是谁在调控 exon7 是否被剪掉? 研究者首先利用 RBP motif 数据库和序列分析工具,在 exon7 及其邻近内含子区域寻找潜在的 RNA 结合蛋白(RBP)结合位点。结果发现,该区域存在多个 SRSF9 的典型结合 motif。同时在临床样本中观察到 SRSF9 在口腔癌组织中显著高表达,并且其表达水平与 exon7 skipping 的比例呈正相关。这些证据提示 SRSF9 可能参与调控 SLC37A4 的剪接选择。 但相关性并不能证明因果关系。为了验证 SRSF9 是否直接调控这一剪接事件,研究者构建了 SLC37A4 exon7 的 minigene 剪接报告系统。
在这一实验中,研究者将 exon7 及其上下游内含子序列克隆到一个剪接报告载体中。该载体设计为 EGFP / RFP 双荧光报告系统:当 exon7 被跳过(exon skipping) 时,报告基因阅读框保持完整,细胞会产生明显的荧光信号;而当 exon7 被保留(exon inclusion) 时,阅读框被破坏,荧光信号明显降低。通过检测荧光强度或RT-PCR产物,就可以判断剪接模式的变化。 当研究者在细胞中 敲低 SRSF9 时,minigene 报告系统中的荧光信号明显下降。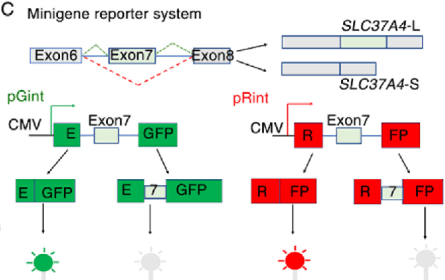
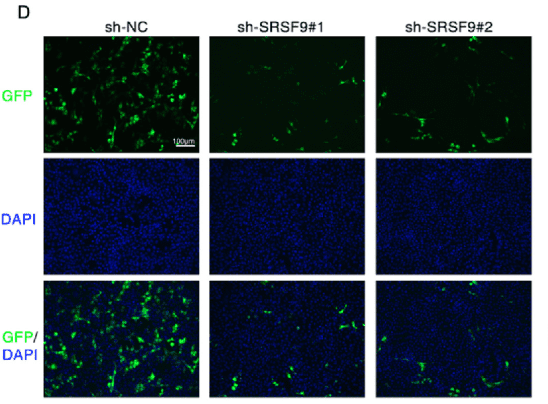
进一步通过 RT-PCR 分析剪接产物发现,exon7 的保留比例显著增加,说明 SRSF9 的缺失会抑制 exon7 的跳跃。
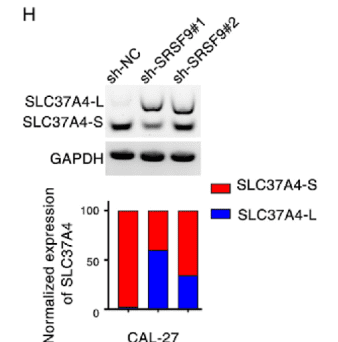
为了进一步验证这一调控是否依赖于特定序列,研究者又构建了 突变型 minigene,将 预测的 SRSF9 结合位点进行点突变。结果显示,在这些结合位点被突变后,即使存在 SRSF9,exon7 的跳跃也明显减少。这说明 SRSF9 必须通过这些特定 RNA motif 才能调控该剪接事件。 通过这一系列实验,研究者最终证明:SRSF9 通过结合 SLC37A4 exon7 周围的 RNA 序列,促进 exon7 skipping,从而产生具有促癌作用的剪接亚型 SLC37A4-S。 这个案例很好地展示了 minigene 在剪接研究中的关键作用:当研究者已经发现一个异常剪接事件,并锁定潜在调控因子后,minigene 可以在细胞中重建这一剪接过程,通过序列突变或RBP操作,直接验证剪接调控机制。 也正因为如此,在许多 RNA 剪接研究论文中,我们几乎都会看到这样一条经典技术路径: 剪接事件发现 → 调控因子预测 → minigene 机制验证。一个完整的 minigene :实验通常如何完成?
在论文中,minigene实验往往只占一两张图,但实际上,从设计到结果解析往往需要经历一整套实验流程。 一个典型的 minigene 验证实验通常包括几个关键步骤。
在 minigene 实验中,研究者将包含目标外显子及其上下游内含子序列的 DNA 片段克隆至表达载体中,构建 minigene 报告系统。该载体转染至细胞后,在细胞内转录产生 pre-mRNA,并经历 RNA 剪接。随后通过 RT-PCR 和凝胶电泳检测不同剪接产物,从而比较不同序列或突变对剪接模式的影响,为解析 RNA 剪接调控机制提供实验依据。
1. 剪接区域设计 首先需要确定需要验证的剪接区域。 一般来说,一个有效的 minigene 构建通常需要包含: 目标外显子 上下游部分内含子 邻近外显子 内含子区域过短可能丢失重要调控元件,而过长又会增加构建难度,因此设计阶段往往需要结合 基因结构信息与剪接位点预测 来确定合适范围。 2. minigene 载体构建 确定目标区域后,需要将该 DNA 片段克隆到剪接报告载体中。 在很多研究中,还会同时构建多个版本,例如: 野生型序列 突变型序列 删除某些调控元件的构建体 通过这些构建体之间的比较,可以解析不同序列对剪接的影响。 3. 细胞转染与表达 构建好的 minigene 载体需要转染到细胞中表达。 常见使用的细胞系包括: HEK293T HeLa 或与研究对象相关的细胞模型 如果研究者希望验证某个 RBP 的作用,还可以进行: RBP 过表达 RBP knockdown 从而观察剪接结果是否发生改变。 4. 剪接结果检测 转染一定时间后,研究者会提取 RNA 并进行 RT-PCR 检测。 不同剪接形式通常会产生不同长度的 PCR 产物,因此可以通过: 凝胶电泳 Sanger测序 或高通量测序 来确认剪接结果。 通过比较不同构建体之间的剪接比例变化,就可以判断: 某个序列是否影响剪接 某个突变是否改变剪接模式 某个RBP是否参与调控
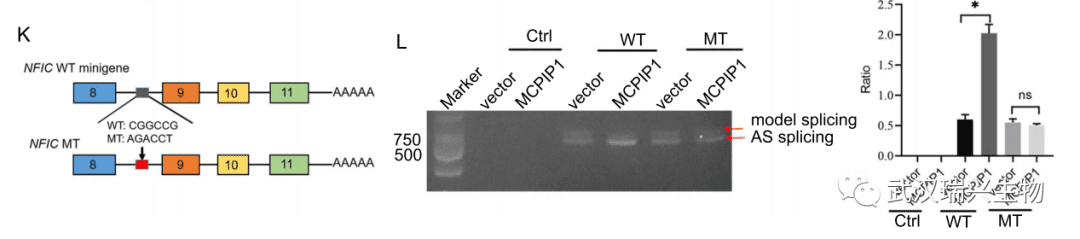
我司minigene验证实验的技术服务 客户提供: 感兴趣的待检基因,RNA-seq数据,iRIP/CLIP-seq数据 结果交付: 1)minigene构建的质粒 2)minigene序列设计示意图 3)实验报告:实验步骤,原始图片和数据,分析图片和表格,英文材料方法 案例介绍: Chen F, Wang Q, Yu X, et al. MCPIP1-mediated NFIC alternative splicing inhibits proliferation of triple-negative breast cancer via cyclin D1-Rb-E2F1 axis[J]. Cell death & disease, 2021, 12(4): 1-16.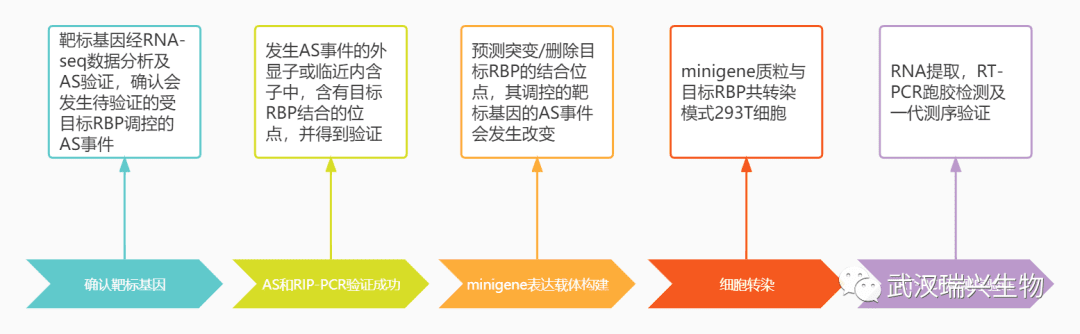
更多细节,欢迎咨询 027-87050299 官网:www.rxbio.cc
![]() 科研之路,与您同行
科研之路,与您同行![]() 若有所获,欢迎点赞、推荐与分享
若有所获,欢迎点赞、推荐与分享
