前言
传统单细胞转录组测序(scRNA-seq)主要依赖短读长平台,能高效回答“哪些基因在哪些细胞中表达”的问题。然而,受限于读长,它难以精确解析同一基因产生的多种RNA异构体(isoform)——这些由可变剪接、可变多聚腺苷酸化等过程产生的转录本多样性,恰恰是高等真核生物功能复杂性的核心来源。近年来,单细胞三代测序技术(单细胞全长转录组)突破技术瓶颈,将转录组分析从“基因级”推向“异构体级”分辨率。那么,这项技术到底能回答哪些传统方法无法触及的科研问题?
细胞类型特异性的异构体使用图谱
同一基因在不同细胞中的“变形记”
过去我们常认为,基因的表达量差异定义了细胞身份。然而,单细胞三代全长转录组揭示:即使是同一基因,在不同细胞类型中会优先使用截然不同的异构体。
在小鼠视网膜研究中,科学家整合短读长与ONT长读长测序,发现超过38%的异构体此前未被注释,且许多异构体呈现细胞类别特异性表达,比如一种Impdh1新异构体在光感受器细胞中占主导地位,而经典异构体表达甚微 [Wang et al., Genome Res, 2025] 。
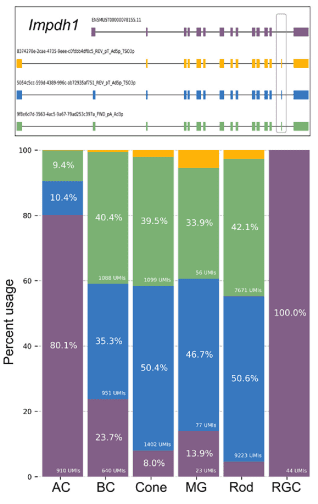
在小鼠心脏研究中,研究者同样观察到,ACTG1基因在成纤维细胞和心肌细胞中使用的异构体截然不同——前者使用蛋白编码型,后者主要使用含内含子保留的非编码型,暗示剪接调控精准匹配细胞类型的功能需求 [Pan et al., Circulation, 2025] 。
这种“同基因不同异构体”的细胞特异性剪接程序,若不依赖全长测序,将被基因表达总量所掩盖。
疾病状态下的异构体“开关”
沉默的致病机制
基因整体表达未变,但其内部异构体比例已悄然倾斜——这种“异构体开关”事件正成为疾病机制研究的新焦点。
在阿尔茨海默病(AD)研究中,单细胞长读长测序发现SEPTIN4基因在AD脑中并无整体表达差异,但其两个异构体发生显著“切换”:一个蛋白编码型异构体下调,另一个新异构体上调,解释了基因层面表达未变的谜团 [Shahnaee et al., Commun Biol, 2026] 。
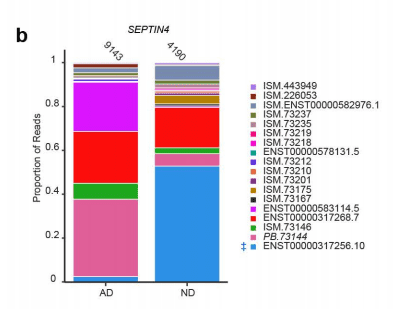
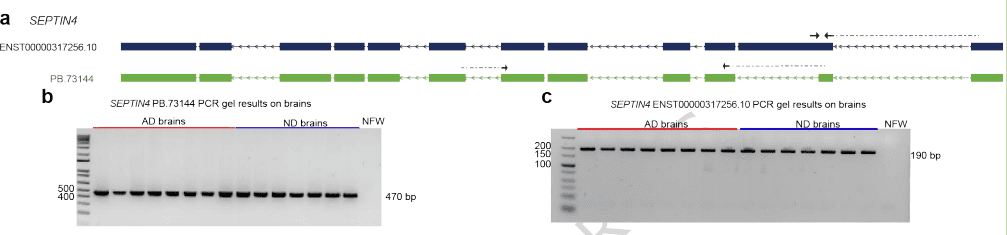
类似现象也出现在结直肠癌(CRC)中,原癌基因MYC在癌细胞中优先使用c-Myc2型异构体,而非c-Myc1型,后者与细胞生长抑制相关 [Lu et al., Protein Cell, 2025] 。
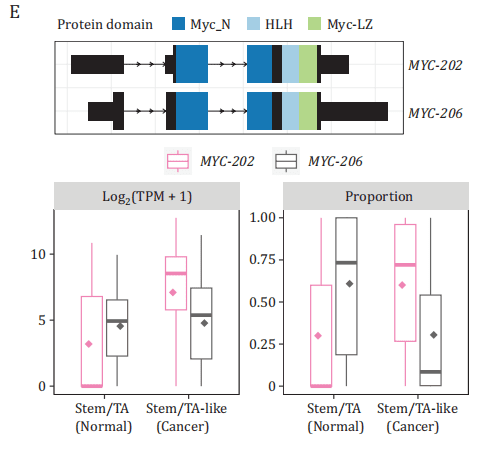
这种从“促增殖”到“抑增殖”的异构体比例倒置,仅靠短读长基因计数无从发现。单细胞三代测序由此成为挖掘功能性剪接变异致病机制的利器。
稀有细胞类型与发育轨迹的精细刻画
同一基因在不同细胞中的“变形记”
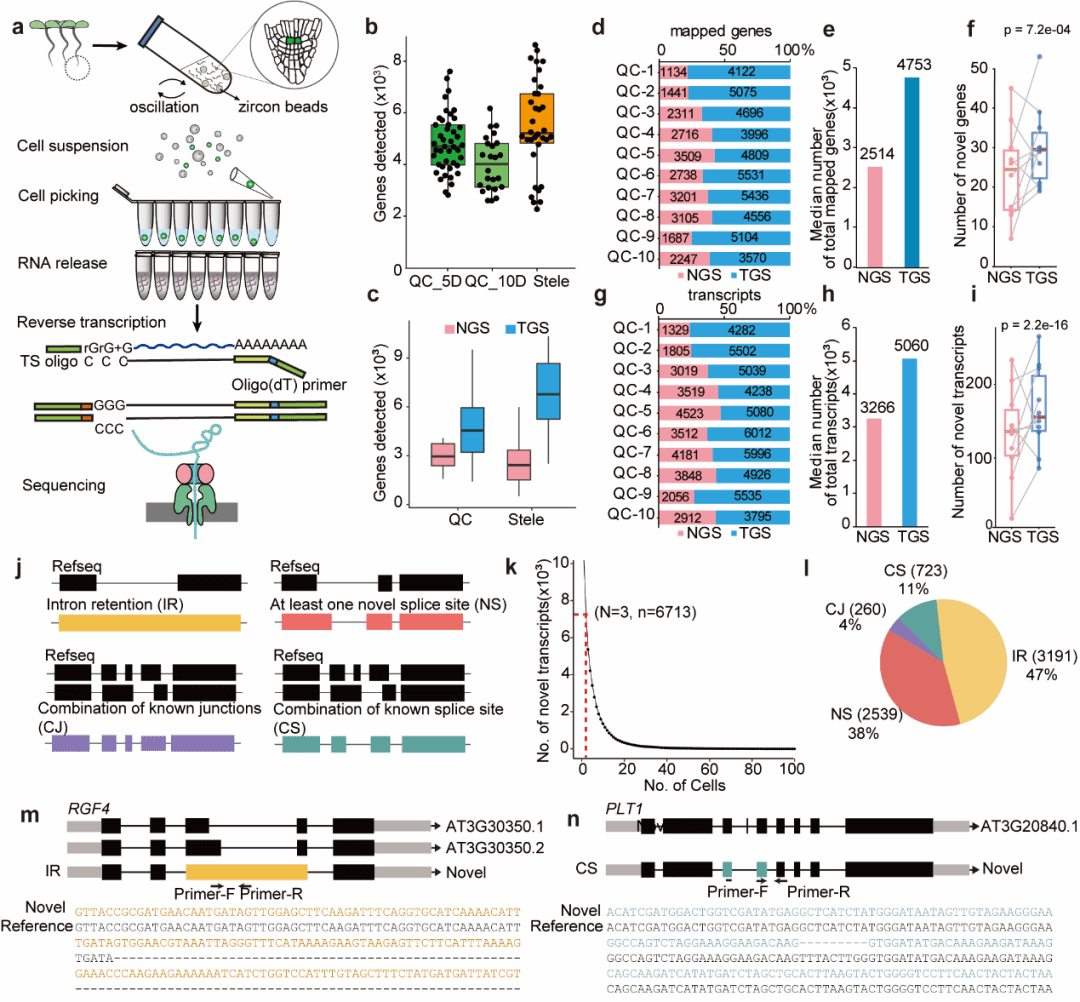
植物根尖的静止中心(QC)细胞数量稀少,维持着干细胞微环境,却难以分离进行转录组分析。借助单细胞三代技术,研究共鉴定出6,713个未注释转录本,包括内含子保留(IR)、新剪接位点(NS)等类型,这些异构体在传统短读长测序中因读长限制无法被完整解析。发现PLT1存在新型CS剪接异构体(9 bp缺失),可能改变蛋白结构域功能;RGF4存在IR型异构体,可能通过无义介导的降解(NMD)调控QC细胞状态。三代数据鉴定的QC标记基因(如WOX5)表达纯度和富集度显著高于已发表的二代单细胞图谱(98.2% vs 8.86%),说明长读长技术能更真实地反映稀有细胞的转录特征。 [Hu et al., Genome Biol, 2026] 。
Genome Biology | 单细胞三代测序揭示植物静止中心的发育轨迹
单细胞三代测序突破了短读长无法解析全长异构体和未注释转录本的瓶颈,为稀有细胞类型的转录本异构体动态和发育轨迹提供了全新分辨率。
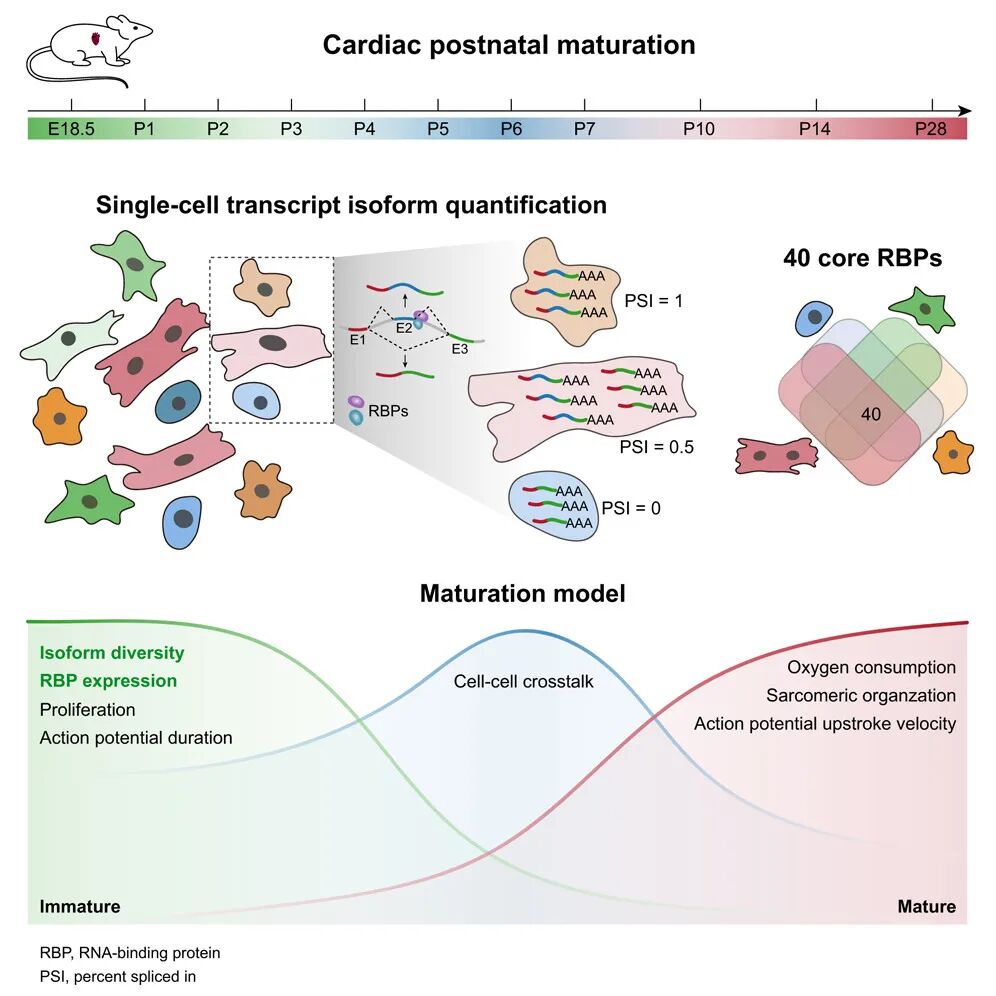
同样,在人类心脏研究中,单细胞三代测序发现 AS模式相比基因表达水平能更精准地定义心脏发育阶段(P1-P28),且在所有主要细胞类型(心肌细胞、成纤维细胞、内皮细胞等)中呈现同步化的年龄依赖性转变。基于完整异构体信息,研究筛选并验证了NCBP2、G3BP1、PTBP1等RBP通过直接结合剪接靶点,在全器官范围内统一调控心脏成熟。识别NCBP2这一在以往研究中未被重视的RBP。功能实验证实,过表达Ncbp2可通过改变关键基因(如Camk2d、Ttn)的可变剪接,在体内显著阻滞心脏成熟 [Li et al., Dev Cell, 2025] 。
单细胞三代测序有效解析全长异构体及动态可变剪接的技术瓶颈,使得从全器官、多细胞类型层面揭示统一的后天心脏成熟调控机制成为可能。
肿瘤异质性的“异构体视角”
新抗原、融合基因与亚克隆进化
癌症基因组的高度异质性一直是治疗难点。单细胞三代测序为解析肿瘤亚克隆结构和转录表型提供了全新维度:
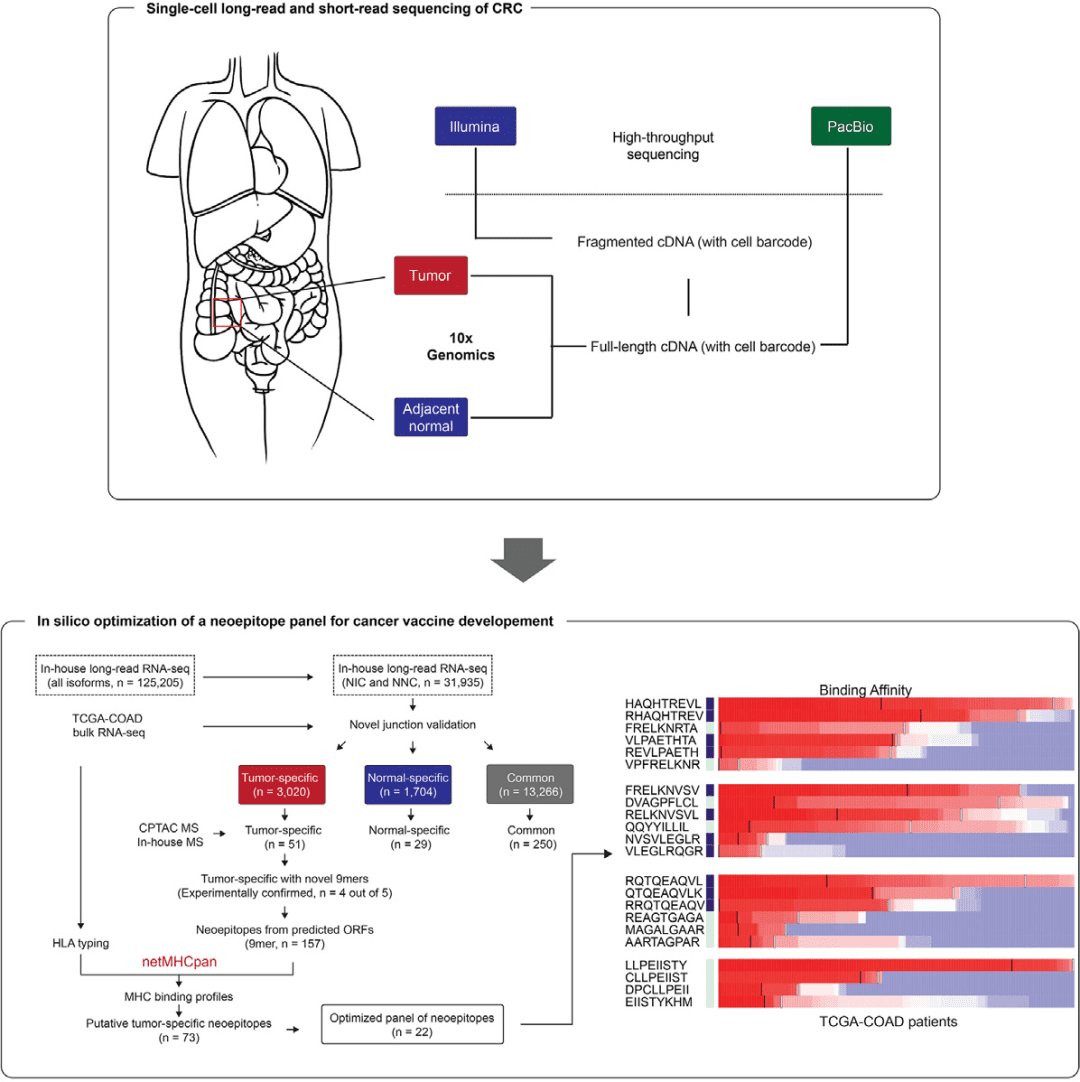
新抗原挖掘:CRC研究中,通过识别肿瘤特异性新异构体及其开放阅读框,研究者筛选出22个能被患者MHC分子呈递的潜在新抗原肽段,为开发通用型癌症疫苗奠定基础 [Li et al., Cell Genom, 2024] 。
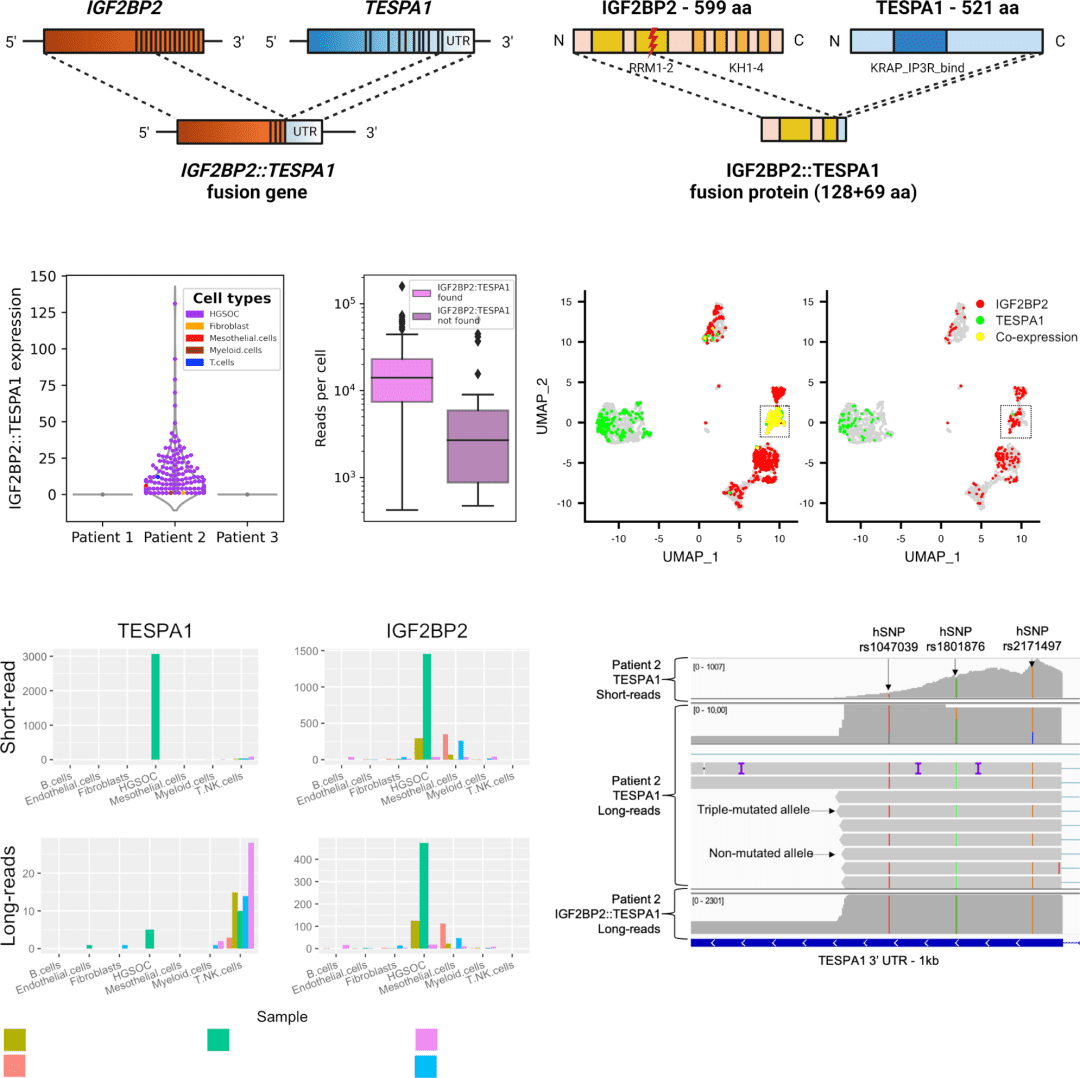
融合基因鉴定:在卵巢癌中,长读长测序发现一个IGF2BP2::TESPA1融合基因,其在短读长数据中被误判为TESPA1高表达,凸显了三代测序在准确检出结构变异方面的优势 [Dondi et al., Nat Commun, 2023] 。
亚克隆解析:慢性淋巴细胞白血病(CLL)研究将长读长测序与基因分型结合,直接观察到BTK耐药突变与不同CLL驱动突变(如DICER1、NOTCH1)在同一细胞中的共存情况,解析了亚克隆演化路径 [Black et al., Genome Res, 2025] 。
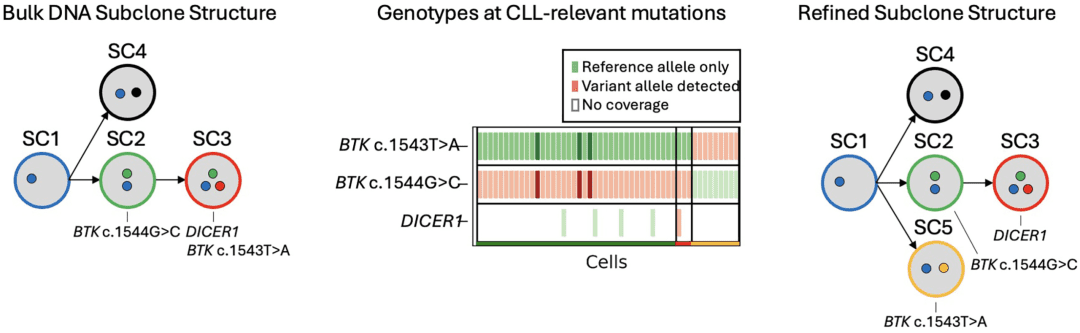
突破中心法则迷雾
直接连接异构体与翻译调控
mRNA表达不等于蛋白质产出。Ribo-STAMP技术结合单细胞三代测序,首次在单细胞和异构体水平上测量核糖体翻译效率。在小鼠海马体研究中,科学家发现Cadm3基因的两个异构体中,长3‘UTR版本在神经元中翻译效率更高,且富集了神经元特异性RNA结合蛋白nELAVL的结合位点 [Sison et al., Nature, 2026] 。
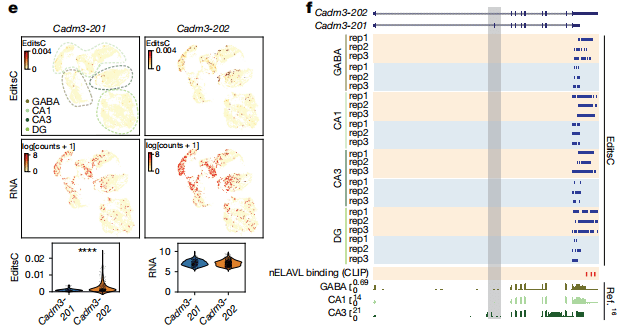
这种“转录-翻译”解偶联现象广泛存在,而长读长测序是分辨“哪个异构体真正被翻译”的唯一手段。
揭示转录后调控的全局图景
从APA到RNA编辑
单细胞三代测序还能全景式地展现3’UTR长度变化(APA)、内含子保留、RNA编辑等转录后事件。
例如,CRC研究显示癌细胞普遍存在3‘UTR缩短现象,且与增殖活性更高的干细胞样细胞群高度相关,以CD44、ARIH2、CSDE1、CYB5B为例,直观显示短 3′UTR 亚型丢失 miRNA 结合位点、表达上调,提示这种剪接变化可能通过逃脱miRNA抑制来促进癌基因表达 [Lu et al., Protein Cell, 2025] 。
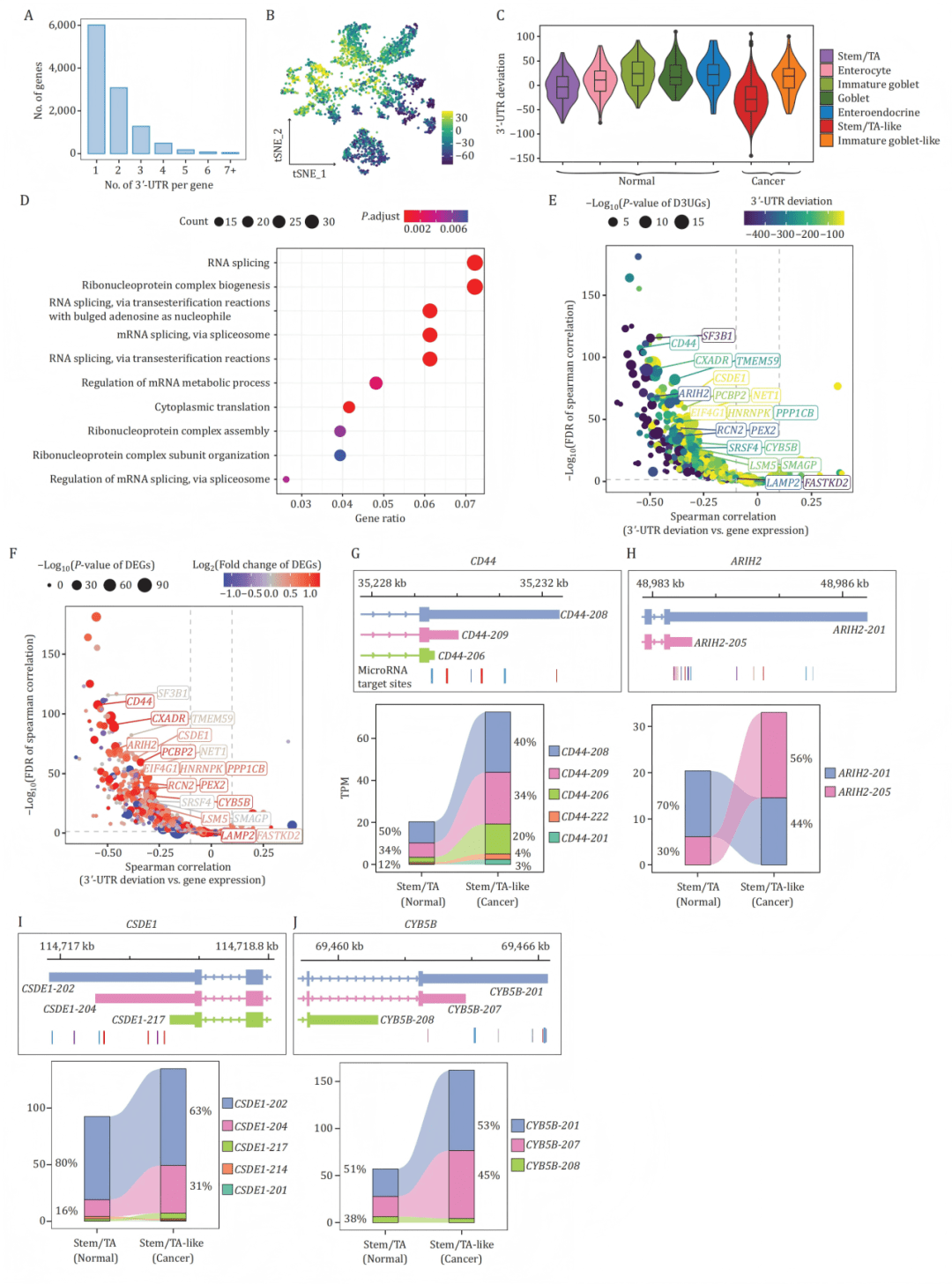
在小鼠心脏中,研究者则发现内含子保留型异构体在心肌细胞中异常丰富,构成了一种细胞特异的翻译缓冲机制 [Pan et al., Circulation, 2025] 。
在小鼠大脑中,长读长测序更是描绘出不同脑区和发育阶段外显子剪接的精细调控网络 [Joglekar et al., Nat Neurosci, 2024] 。
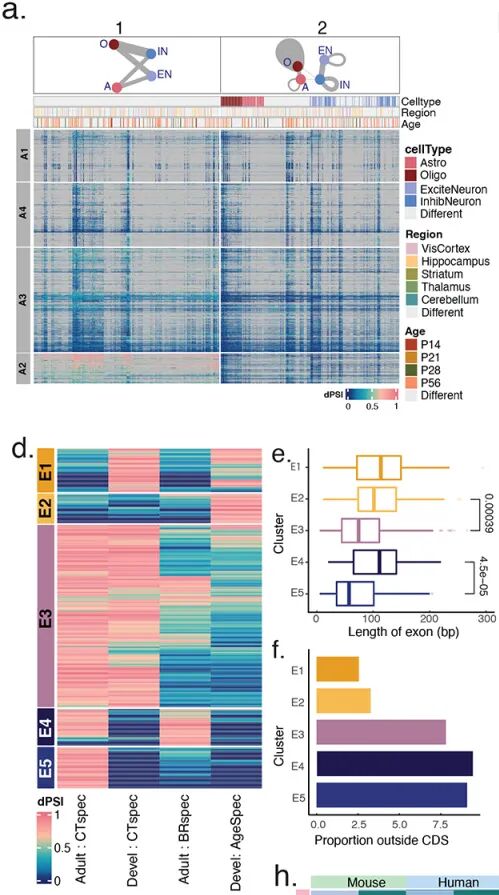
从“看得到”到“看得全”
单细胞三代测序正在推动生命科学从 “基因表达计数” 迈入 “转录组结构解析” 的新阶段。
它不仅能回答“基因在哪儿表达”,更能追问“表达的是哪个版本”、“版本如何切换”、“切换带来何种功能后果”。
对于发育轨迹追踪、疾病机制挖掘、新抗原发现和细胞图谱绘制而言,这项技术提供了前所未有的深度与精度。随着通量提升和成本下降,全长异构体分辨率的单细胞图谱将成为理解复杂生命系统的黄金标准。
更多了解
单细胞三代测序是什么? 一文看懂 scRNA-seq 到 scIso-seq 的技术升级
参考文献:
Hu G, Li C, Guo W, et al. Single-cell transcriptomic analysis of plant quiescent center by third-generation sequencing reveals developmental trajectories. Genome Biol, 2026.
Wang M, Li Y, Wang J, et al. Integrating short-read and long-read single-cell RNA sequencing for comprehensive transcriptome profiling in mouse retina. Genome Res, 2025.
Pan T, Lu L, Yang K, et al. Single-Cell Splicing Isoform Atlas of the Adult Human Heart and Heart Failure. Circulation, 2025.
Li Z, Cao C, Zhao Q, et al. RNA splicing controls organ-wide maturation of postnatal heart in mice. Dev Cell, 2025.
Shahnaee A, Liu CS, Ngo T, et al. RNA isoform diversity, splicing variants and switching in single cells of the Alzheimer’s disease brain. Commun Biol, 2026.
Lu P, Zhang Y, Cui Y, et al. Systematic characterization of full-length RNA isoforms in human colorectal cancer at single-cell resolution. Protein Cell, 2025.
Li Z, Zhang B, Chan JJ, et al. An isoform-resolution transcriptomic atlas of colorectal cancer from long-read single-cell sequencing. Cell Genom, 2024.
Dondi A, Lischetti U, Jacob F, et al. Detection of isoforms and genomic alterations by high-throughput full-length single-cell RNA sequencing in ovarian cancer. Nat Commun, 2023.
Black GS, Huang X, Qiao Y, et al. Long-read single-cell RNA sequencing enables the study of cancer subclone-specific genotypes and phenotypes in chronic lymphocytic leukemia. Genome Res, 2025.
Sison SL, Zampa F, Kofman ER, et al. Single-cell and isoform-specific translational profiling of the mouse brain. Nature, 2026.
Joglekar A, Hu W, Zhang B, et al. Single-cell long-read sequencing-based mapping reveals specialized splicing patterns in developing and adult mouse and human brain. Nat Neurosci, 2024.
更多了解,欢迎咨询:027-87050299
