RXBio Translates Sequence to Science and Industry
Tel: 027-87050299Email: sales@rxbio.cc
RXBio Translates Sequence to Science and Industry
M6A修饰在人转录组RNA中广泛存在,目前研究表明:超过7000个mRNA和300个IncRNA都含有这种修饰; 这种修饰富集分布在mRNA的终止密码子附近和3’UTR区域,暗示m6A修饰具有重要的调控功能。 很多m6A修饰位点在人和小鼠中保守存在,且某些m6A修饰在不同发育时期,其修饰水平也在不断变化,同样暗示其重要的调控功能。
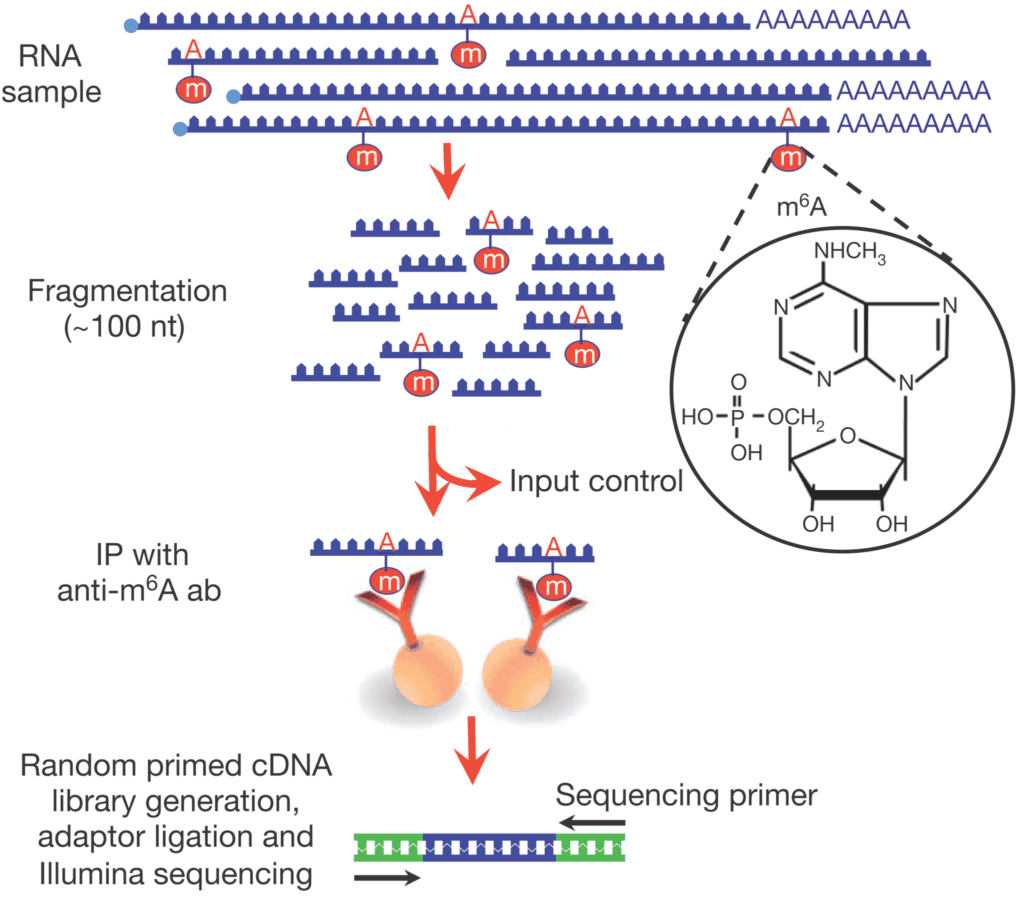
目前对m6A的全基因组研究方法为meRIP-seq,其原理为通过特异识别m6A修饰的抗体,对细胞内具有m6A修饰的RNA片段进行免疫共沉淀通过对沉淀下来的RNA片段进行高通量测序,进而结合生物信息学分析,即可在全基因组范围内对m6A修饰的状况进行系统研究。
✔ 针对不同研究领域提供个性化方案;
✔ 分析流程全备,数据解读详细,后期数据挖掘可提供个性化分析;
✔ 结合峰分析策略多种:含Ablife和Piranha两种方法;
✔ 研究思路丰富:m6A修饰图谱及修饰特征分析,不同实验分组间差异m6A修饰位点和基因鉴定; 与RNA-seq、CLIP-seq数据等联合分析,揭示m6A修饰的功能。
-1024x380.png)
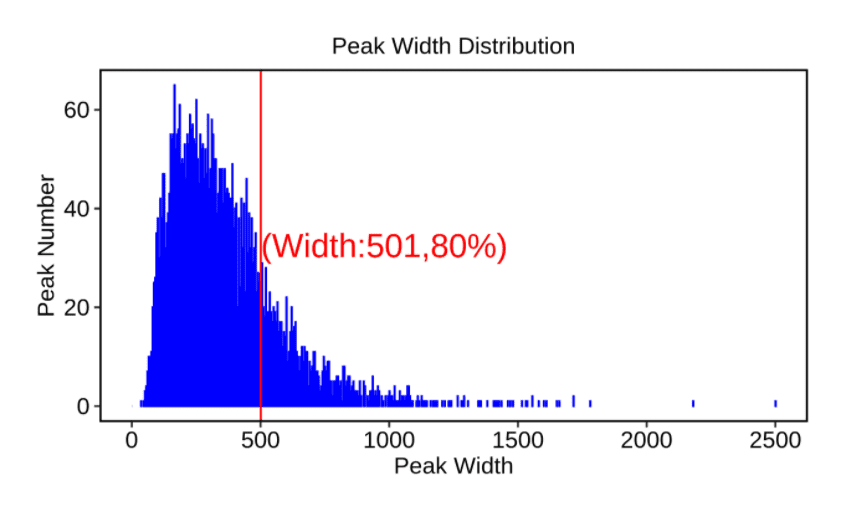
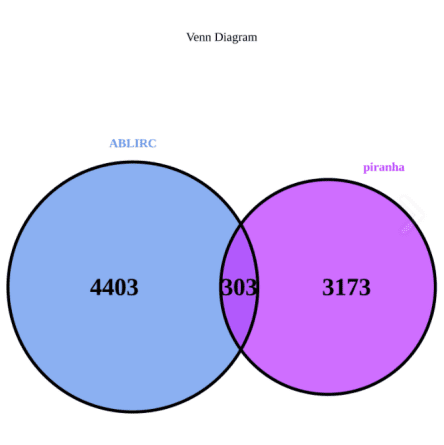

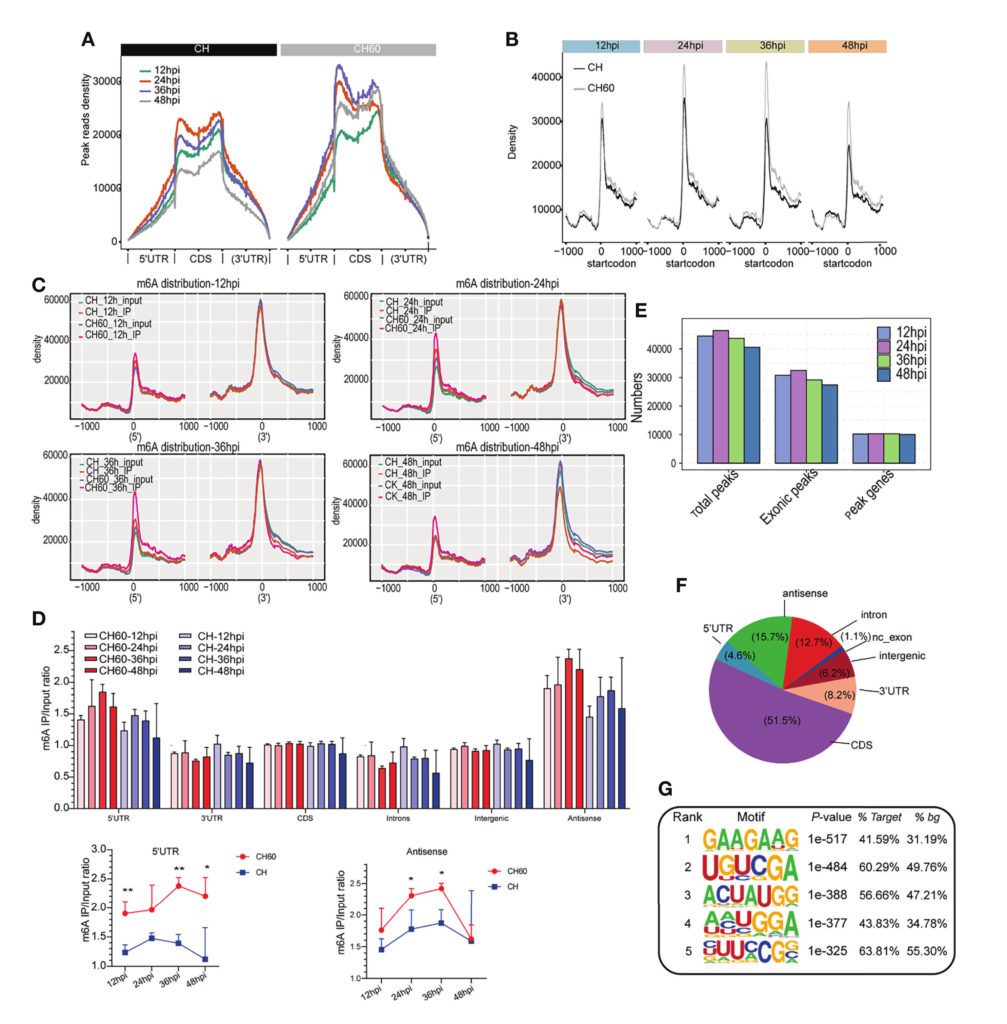
通过对强毒性和弱毒性的鸭甲肝病毒(DHAV)感染的雏鸭肝脏组织进行m6A-seq测序,首次分析了鸭子mRNA上的m6A修饰水平及分布特征,发现GAAGAAG是修饰基序最丰富的基序,整合分析m6A-seq和RNA-seq数据,发现m6A与DHAV感染雏鸭肝脏中mRNA表达水平总体呈正相关(Wu etal.2022)。

电话:027-870502099
邮箱:sales@rxbio.cc
地址:武汉市东湖高新区高新二路388 号
光谷生物医药加速器 18 栋 1-2层
单细胞多组学 空间转录组
三代测序 功能基因组
表观遗传学 互作组学
单细胞大数据 数据深度挖掘

欢迎关注公众号「瑞兴生物」